Holmijs, atomskaitlis 67, atomsvars 164,93032, elementa nosaukums atvasināts no atklājēja dzimšanas vietas.
Satursholmijsgarozā ir 0,000115%, un tas pastāv kopā ar citiemretzemju elementimonacītā un retzemju minerālos. Dabīgais stabilais izotops ir tikai holmijs 165.
Holmijs ir stabils sausā gaisā un ātri oksidējas augstā temperatūrā;Holmija oksīdsir zināms, ka tam piemīt visspēcīgākās paramagnētiskās īpašības.
Holmija savienojumu var izmantot kā piedevu jauniem feromagnētiskiem materiāliem; Holmija jodīdu izmanto metālu halogenīdu lampu ražošanā.holmija lampas, un holmija lāzeri tiek plaši izmantoti arī medicīnas jomā.

Vēstures atklāšana
Atklājējs: Dž. L. Sorets, PT Klīvlenda
Atklāts no 1878. līdz 1879. gadam
Atklāšanas process: atklāja J. L. Sorets 1878. gadā; atklāja P. T. Klīvs 1879. gadā
Pēc tam, kad Mosandrs atdalīja erbija zemi unterbijszeme noitrijszeme 1842. gadā daudzi ķīmiķi izmantoja spektrālo analīzi, lai identificētu un noteiktu, ka tie nav tīri elementa oksīdi, kas mudināja ķīmiķus turpināt to atdalīšanu. Pēc iterbija oksīda unskandija oksīds1879. gadā Klifs no oksidētas ēsmas atdalīja divus jaunus elementu oksīdus. Viens no tiem ir nosaukts par Holmiju, lai pieminētu Klifa dzimšanas vietu, seno latīņu nosaukumu Holmia Stokholmā, Zviedrijā, ar elementa simbolu Ho. 1886. gadā Buvabadrands no holmija atdalīja vēl vienu elementu, bet nosaukums holmijs tika saglabāts. Atklājot holmiju un citus retzemju elementus, ir pabeigts vēl viens retzemju elementu trešā atklāšanas posms.
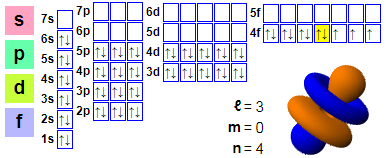
Elektroniskais izkārtojums:
Elektroniskais izkārtojums:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f11
Tas ir metāls, kas, tāpat kā disprozijs, var absorbēt neitronus, kas rodas kodolu skaldīšanas rezultātā.
Kodolreaktorā, no vienas puses, tiek veikta nepārtraukta sadegšana, un, no otras puses, tiek kontrolēts ķēdes reakcijas ātrums.
Elementa apraksts: Pirmā jonizācijas enerģija ir 6,02 elektronvolti. Tam ir metālisks spīdums. Tas var lēni reaģēt ar ūdeni un šķīst atšķaidītās skābēs. Sāls ir dzeltens. Oksīds Ho2O2 ir gaiši zaļš. Izšķīdinot minerālskābēs, veidojas trīsvērtīgu jonu dzelteni sāļi.
Elementa avots: iegūts, reducējot holmija fluorīdu HoF3 · 2H2O ar kalciju.
Metāls
Holmijs ir sudrabaini balts metāls ar mīkstu tekstūru un plastiskumu; kušanas temperatūra 1474 °C, viršanas temperatūra 2695 °C, blīvums 8,7947 g/cm³ holmija metrs³.
Holmijs ir stabils sausā gaisā un ātri oksidējas augstās temperatūrās; Ir zināms, ka holmija oksīdam piemīt visspēcīgākās paramagnētiskās īpašības.
Savienojumu iegūšana, ko var izmantot kā piedevas jauniem feromagnētiskiem materiāliem; Holmija jodīds, ko izmanto metālhalogenīdu lampu ražošanā – holmija lampas
Pieteikums
(1) Kā piedeva metālu halogenīdu lampām, metālu halogenīdu lampas ir gāzizlādes lampu veids, kas izstrādāts uz augstspiediena dzīvsudraba lampu bāzes, un tām raksturīga spuldzes piepildīšana ar dažādiem retzemju halogenīdiem. Pašlaik galvenais pielietojums ir retzemju jodīds, kas gāzizlādes laikā izstaro dažādas spektrālās krāsas. Holmija lampās izmantotā darba viela ir holmija jodīds, kas var sasniegt augstu metālu atomu koncentrāciju loka zonā, ievērojami uzlabojot starojuma efektivitāti.
(2) Holmiju var izmantot kā piedevu itrija dzelzs vai itrija alumīnija granātam.
(3) Ar Ho:YAG leģēts itrija alumīnija granāts var izstarot 2 μM lāzeru cilvēka audos uz 2 μ. M lāzera absorbcijas ātrums ir augsts, gandrīz par trim lieluma kārtām augstāks nekā Hd:YAG. Tātad, izmantojot Ho:YAG lāzeru medicīniskajā ķirurģijā, var ne tikai uzlabot ķirurģisko efektivitāti un precizitāti, bet arī samazināt termiskā bojājuma laukumu. Holmija kristālu radītais brīvais stars var likvidēt taukus, neradot pārmērīgu karstumu, tādējādi samazinot termiskos bojājumus veseliem audiem. Tiek ziņots, ka holmija lāzera ārstēšana glaukomas ārstēšanai Amerikas Savienotajās Valstīs var mazināt pacientu sāpes, kuriem tiek veikta operācija. Ķīnā 2 μ M lāzera kristālu līmenis ir sasniedzis starptautisku līmeni, un jāpieliek pūles, lai izstrādātu un ražotu šāda veida lāzera kristālus.
(4) Magnetostriktīvajā sakausējumā Terfenol D var pievienot arī nelielu daudzumu holmija, lai samazinātu ārējo lauku, kas nepieciešams sakausējuma piesātinājuma magnetizācijai.
(5) Izmantojot ar holmiju leģētu šķiedru, var izveidot optiskās sakaru ierīces, piemēram, šķiedru lāzerus, šķiedru pastiprinātājus un šķiedru sensorus, kam būs nozīmīgāka loma mūsdienu šķiedru optikas sakaru straujajā attīstībā.
(6) Holmija lāzera litotripsijas tehnoloģija: medicīniskā holmija lāzera litotripsija ir piemērota cietu nierakmeņiem, urīnvadu akmeņiem un urīnpūšļa akmeņiem, kurus nevar salauzt ar ekstrakorporālu triecienviļņu litotripsiju. Izmantojot medicīnisko holmija lāzera litotripsiju, medicīniskā holmija lāzera tievā šķiedra tiek izmantota, lai caur urīnizvadkanālu un urīnvadu, izmantojot cistoskopu un ureteroskopu, tieši sasniegtu urīnpūsli, urīnvadu un nierakmeņus. Pēc tam uroloģijas speciālisti manipulē ar holmija lāzeru, lai salauztu akmeņus. Šīs holmija lāzera ārstēšanas metodes priekšrocība ir tā, ka tā var izārstēt urīnvadu akmeņus, urīnpūšļa akmeņus un lielāko daļu nierakmeņu. Trūkums ir tāds, ka dažiem akmeņiem augšējā un apakšējā nieru kausā var būt neliels daudzums atlikušo akmeņu, jo holmija lāzera šķiedra, kas iekļūst no urīnvada, nespēj sasniegt akmens vietu.
Publicēšanas laiks: 2023. gada 16. augusts