Lutēcijsir retzemju elements ar augstām cenām, minimālām rezervēm un ierobežotu izmantošanu. Tas ir mīksts un šķīst atšķaidītās skābēs, un var lēni reaģēt ar ūdeni.
Dabā sastopamie izotopi ir 175Lu un tā pussabrukšanas periods ir 2,1 × 10^10 gadi. β emitētājs ir 176Lu. To iegūst, reducējot lutēcija(III) fluorīdu LuF∨ · 2H₂O ar kalciju.
Galvenais pielietojums ir kā katalizators naftas krekinga, alkilēšanas, hidrogenēšanas un polimerizācijas reakcijām; Turklāt lutēcija tantalātu var izmantot arī kā rentgenstaru fluorescējoša pulvera materiālu; 177Lu, radionuklīdu, var izmantot audzēju staru terapijai.

Vēstures atklāšana
Atklājējs: G. Urbans
Atklāts 1907. gadā
Lutēciju no iterbija 1907. gadā atdalīja franču ķīmiķis Ulbans, un tas arī bija retzemju elements, kas tika atklāts un apstiprināts 20. gadsimta sākumā. Lutēcija latīņu nosaukums cēlies no senā Parīzes, Francijas, nosaukuma, kas ir Urbana dzimšanas vieta. Lutēcija un vēl viena retzemju elementa - europija - atklāšana noslēdza visu dabā sastopamo retzemju elementu atklāšanu. To atklāšanu var uzskatīt par ceturto vārtu atvēršanu retzemju elementu atklāšanā un retzemju elementu atklāšanas ceturtā posma pabeigšanu.
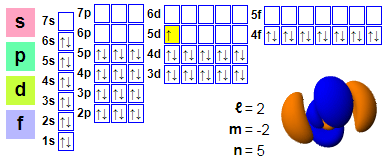
Elektronu konfigurācija
Elektroniskie pasākumi:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d1
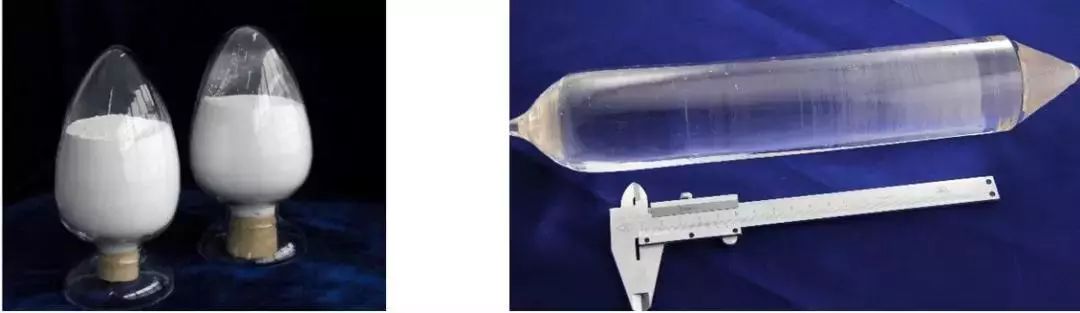
Lutēcijs ir sudrabaini balts metāls, kas ir cietākais un blīvākais metāls starp retzemju elementiem; kušanas temperatūra 1663 ℃, viršanas temperatūra 3395 ℃, blīvums 9,8404. Lutēcijs ir relatīvi stabils gaisā; lutēcija oksīds ir bezkrāsains kristāls, kas šķīst skābēs, veidojot atbilstošus bezkrāsainus sāļus.
Lutēcija retzemju metālu spīdums ir starp sudrabu un dzelzi. Piemaisījumu saturam ir būtiska ietekme uz to īpašībām, tāpēc literatūrā bieži vien ir ievērojamas atšķirības to fizikālajās īpašībās.
Metāliem itrijam, gadolīnijam un lutēcijam ir spēcīga izturība pret koroziju un tie ilgstoši var saglabāt savu metālisko spīdumu.
Pieteikums
Ražošanas grūtību un augsto cenu dēļ lutēcijam ir maz komerciālu pielietojumu. Lutēcija īpašības būtiski neatšķiras no citiem lantanīdu metāliem, taču tā rezerves ir relatīvi mazākas, tāpēc daudzviet lutēcija aizstāšanai parasti izmanto citus lantanīdu metālus.
Lutēciju var izmantot dažu īpašu sakausējumu izgatavošanai, piemēram, lutēcija alumīnija sakausējumu var izmantot neitronu aktivācijas analīzei. Lutēciju var izmantot arī kā katalizatoru naftas krekingā, alkilēšanas, hidrogenēšanas un polimerizācijas reakcijās. Turklāt lutēcija dopēšana dažos lāzerkristālos, piemēram, itrija alumīnija granātā, var uzlabot tā lāzera veiktspēju un optisko vienmērīgumu. Turklāt lutēciju var izmantot arī fosforu ražošanā: lutēcija tantalāts ir pašlaik zināmais kompaktais baltais materiāls un ideāls materiāls rentgenstaru fosforiem.
177Lu ir sintētisks radionuklīds, ko var izmantot audzēju staru terapijai.
Lutēcija oksīdsleģēts cērija itrija lutēcija silikāta kristāls
Publicēšanas laiks: 2023. gada 26. jūnijs